
Закон Менделеева–Клапейрона можно записать в виде PV=νRT, где P — давление (в паскалях), V — объём (в м3 ), ν — количество вещества (в молях), T — температура (в градусах Кельвина), а R — универсальная газовая постоянная, равная 8,31 Дж/(К*моль). Пользуясь этой формулой, найдите температуру T (в градусах Кельвина), если ν=3,1 моль, P=6440,25 Па, V=1,8 м3.
PV=νRT
T=(PV)/(νR)
T=(6440,25*1,8)/(3,1*8,31)
T=(644025*18)/(31*831)
T=(644025*(6*3))/(31*(277*3))
T=(644025*6)/(31*277)
T=((20775*31)*6)/(31*277)
T=(20775*6)/277
T=((75*277)*6)/277
T=75*6=450
Ответ: 450
Поделитесь решением
Присоединяйтесь к нам...
Решите уравнение (x-2)2(x-3)=20(x-2).
Упростите выражение (6b-8)(8b+6)-8b(6b+8) и найдите его значение при b=-8,2. В ответе запишите найденное значение.
Центростремительное ускорение при движении по окружности (в м/с2) вычисляется по формуле a=ω2R, где ω — угловая скорость (в с-1), R — радиус окружности (в метрах). Пользуясь этой формулой, найдите радиус R, если угловая скорость равна 9c-1, а центростремительное ускорение равно 243м/с2. Ответ дайте в метрах.
Упростите выражение 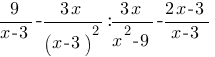
Мощность постоянного тока (в ваттах) вычисляется по формуле P=I2R, где I — сила тока (в амперах), R — сопротивление (в омах). Пользуясь этой формулой, найдите сопротивление R, если мощность составляет 588 Вт, а сила тока равна 7 А. Ответ дайте в омах.
Комментарии: